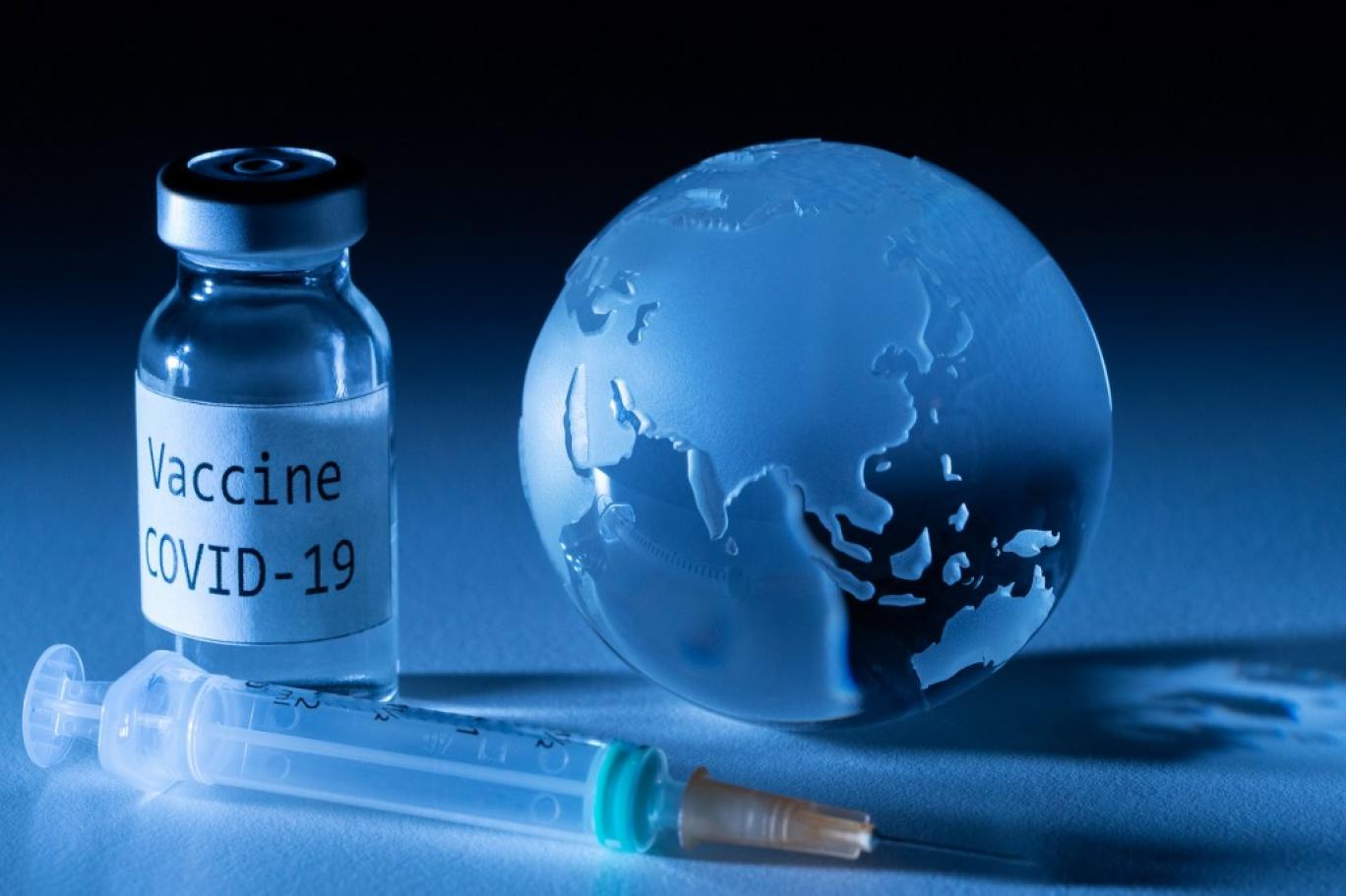
شرکت فایزر و همکار آلمانی آن، شرکت بایونتک، از سازمانهای مقرراتی اتحادیه اروپا درخواست اخذ مجوز استفاده اضطراری برای واکسن کووید-۱۹ خود کردند که پیشبینی میشود راه را برای عرضه آن در سراسر این قاره هموار کند.
این شرکتها پا در راه مدرنا گذاشتهاند که پیشتر از آژانس دارویی اتحادیه اروپا درخواست مجوز کرده بود و از ۶ اکتبر نتایج آزمایشهای خود را برای بررسیهای چرخشی در اختیار این سازمان قرار داده بود.
آژانس دارویی اتحادیه اروپا گفت، نهایتا تا ۲۹ دسامبر جلسهای برگزار خواهد کرد تا تشخیص دهد که آیا این واکسنها به اندازه کافی ایمن و کارآمد هستند تا مجوز لازم را دریافت کنند. این سازمان اضافه کرد که ممکن است به زودی در ۱۲ ژانویه، واکسن تولیدی مدرنا را تایید کند.
درخواست فایزر و بایونتک از آژانس دارویی اتحادیه اروپا، بعد از درخواست تایید آنان از ایالات متحده در ۲۰ نوامبر ثبت شد و این اقدام، آنها را یک قدم به عرضه واکسن خود نزدیکتر کرده است.
اطلاعات موجود از آزمایشهای بالینی و گسترده فایزر نیز هفته گذشته به آژانس قانونگذاری محصولات پزشکی و بهداشتی بریتانیا ارائه شد تا از این سازمان هم برای واکسن خود مجوز دریافت کند.
آلبرت برولا، مدیرعامل فایزر، روز سهشنبه با صدور بیانیهای اظهار داشت: «ما از آغاز روند تولید واکسن میدانیم که بیماران منتظر آن هستند و ما هم آمادهایم تا واکسن کووید-۱۹ خود را به محض اخذ مجوز لازم از مقامات، ارسال کنیم.»
وزیر علوم آلمان گفت که استانداردهای ایمنی همیشگی درباره روند تایید واکسنهای ویروس کرونا نیز همانطور که برای سایر داروها استفاده میشود، به کار بسته شده است و این امر، نکتهای کلیدی در افزایش هرچه بیشتر مقبولیت و پذیرش مصونیت این واکسن در بین عموم مردم خواهد بود.
آنیا کارلیشک به خبرنگاران در برلین گفت که آژانس دارویی اتحادیه اروپا جلسهای علنی در ۱۱ دسامبر برگزار خواهد کرد تا درخواست تایید بایونتک و فایزر را بررسی کند.
آخرین ارزیابی از این واکسن که ماه گذشته منتشر شد، نشان داد که ایمن است و در جلوگیری از ابتلا به کووید-۱۹ تا ۹۵ درصد موثر است.
مرحله سوم آزمایش فایزر شاهد حضور بیش از ۴۰ هزار داوطلب از سراسر دنیا بود. ۴۲ درصد از شرکتکنندگان متعلق به گروههای متنوع نژادی بودند و ۴۱ درصد بین ۵۶ تا ۸۵ سال سن داشتند.
فایزر گفت که واکنش ایمنی مناسبی میان افراد واکسنزده «از هر سن، جنسیت، نژاد و قومیت» پدیدار شده است و این واکسن در پیشگیری از ابتلا در میان افراد ۶۵ ساله و مسنتر نیز بیش از ۹۴ درصد کارآمد است.
Read More
This section contains relevant reference points, placed in (Inner related node field)
فایزر و بایونتک گفتهاند که هیچ عوارض جانبی جدی در واکسن آنها مشاهده نشده است؛ هر چند بعضی از داوطلبان از سردرد و سرگیجه خبر دادهاند.
در مجموع، در این آزمایش ۱۰ مورد وخیم ابتلا به کووید-۱۹ کشف شد که از آن میان ۹ نفر متعلق به گروه پلاسبو بودند، و تنها یک نفر از آنان واکسن زده بود.
پروفسور اوگور شاهین، دانشمندی که این واکسن را کشف کرد، ماه گذشته گفت که «بسیار مطمئن» است که واکسن همچنین باعث کاهش نرخ ابتلا، شاید حتی تا ۵۰ درصد، شود که به کاهش «شدید» موارد ابتلا خواهد انجامید.
او گفت: «به عنوان یک دانشمند و با توجه به آنچه تاکنون از ویروسهای دیگر شاهد بودهایم، انتظار من این است که نرخ تاثیر بالای واکسن در جلوگیری از ابتلا به بیماری، منجر به مقداری تاثیر بر پیشگیری از ادامه شیوع بیماری هم خواهد شد. اطمینان زیادی دارم که با چنین واکسن کارآمدی، سرایت از مردم به یکدیگر کاهش خواهد یافت. شاید این کاهش ۹۰ درصد نباشد، ولی احتمالا تا ۵۰ درصد کاهش خواهد یافت. و ما نباید فراموش کنیم که حتی همین مقدار نیز باعث کاهش شدید سرایت این بیماری عالمگیر خواهد شد.»
با این حال، او هشدار داد که عرضه واکسن «به این معنی نیست که اوضاع تا پایان سال آینده به شدت تغییر خواهد کرد.»
او گفت: «زمستانی سخت پیش رو خواهیم داشت، اوضاع پیش از آن که بهتر شود، بدتر خواهد شد.»
دولت بریتانیا در مجموع ۴۰ میلیون دُز از این واکسن را خریداری کرده است و اگر این واکسن تایید شود، ۱۰ میلیون از آن قرار است تا پایان سال جاری میلادی به کشور تحویل داده شود.
مصونیت در برابر بیماری ۲۸ روز بعد از تزریق اولین واکسن ایجاد خواهد شد، چرا که این واکسن به تزریق دو دُز با فاصله از هم نیاز دارد و با این روند، طی زمستان پیش رو، تا نزدیک به ۵ میلیون بریتانیایی واکسینه خواهند شد.
پروفسور شاهین، از بنیانگذاران بایونتک، گفت که اطلاعات آنها حاکی از نرخ مصونیت بالا علیه کووید-۱۹ است که «خیلی سریع» بعد از تزریق دُز اول واکسن در بدن ایجاد میشود.
مقامات تاکید کردهاند که عرضه اولیه واکسن محدود خواهد بود. حدود ۵۰ میلیون دُز که برای واکسینه کردن ۲۵ میلیون نفر کافی است، قرار است تا پایان سال جاری میلادی در سراسر جهان عرضه شود.
بعد از آن هم فایزر بنا دارد مجموع ۱.۳ میلیارد دوز از واکسن خود را طی سال ۲۰۲۱ تولید و توزیع کند.
فایزر و بایونتک قراردادی ۱.۴۸ میلیارد پوندی با دولت ایالات متحده دارند تا ۱۰۰ میلیون دُز از واکسن را از همین امسال به آن کشور تحویل دهند. علاوه بر ایالات متحده، این دو شرکت همچنین با اتحادیه اروپا، ژاپن و کانادا نیز قراردادهایی برای عرضه واکسن خود امضا کردهاند.
این واکسن باید تا زمان استفاده در دمای منفی ۷۰ درجه سانتیگراد نگهداری شود تا سلامت و کارآمدی بافتهای ژنتیکی آن حفظ شود.
همین امر هم به نوبه خود باعث پیچیدهتر شدن روند عرضه و توزیع واکسن به پزشکان و خانههای سالمندان میشود که به فناوری یخچالی که برای نگهداری از این واکسن در دمای خیلی پایین نیاز است، دسترسی قطعی ندارند.
© The Independent